
生物相容性是指材料在机体特定部位产生的反应,也就是说某些材料或者药物与人体接触或者植入体内是否能够“兼容”,会不会对我们的人体产生伤害。
ISO10993测试也叫医疗器械生物学评价;目前需要做生物相容性测试的产品一般都是医疗用品,包括医疗器械以及医疗药物,测试所参照的标准主要ISO10993GB/T16886,两种标准的内容基本一致。
ISO10993-1:2018取代了ISO 10993-1:2009,(红色为新增测试项目)
第 1部分ISO10993-1:评价与试验;
第 2部分ISO10993-2:动物保护要求;
第 3部分ISO10993-3:遗传毒性、致癌性和生殖毒性试验;
第 4部分ISO10993-4:与血液相互作用试验选择;
第 5部分ISO10993-5:体外细胞毒性试验;
第 6部分ISO10993-6:植人后局部反应试验;
第 7部分ISO10993-7:环氧乙烷灭菌残留量;
第 8部分ISO10993-8:生物学试验参照材料的选择与定量指南;
第 9部分ISO10993-9:潜在降解产物的定性与定量框架;
第 10部分ISO10993-10:刺激与迟发型(持续型)超敏反应试验;
第 11部分ISO10993-11:全身毒性试验;
第 12部分ISO10993-12:样品制备与参照样品;
第13部分ISO10993-13:聚合物医疗器械的降解产物的定性与定量;
第14部分ISO10993-14:陶瓷降解产物的定性与定量;
第 15部分ISO10993-15:金属与合金降解产物的定性与定量;
第 16部分ISO10993-16:降解产物和可溶出物的毒代动力学研究设计;
第 17部分ISO10993-17:可溶出物允许限量的确立;
第 18部分ISO10993-18:材料化学表征。
第19部分ISO10993-19:材料的物理化学、形态学和地形学特性
第20部分ISO10993-20:医疗器械的免疫毒性测试原则和方法
测试项目比较多,但不是所有的产品都要做全套的测试项目,主要是根据产品的使用方法以及产品的作用性能决定的!目前做的Zui多的测试主要是:
第 5部分:ISO10993-5体外细胞毒性试验;
第 10部分:ISO10993-10刺激与迟发型(持续型)超敏反应试验。
ISO10993-5等同于国标的GB/T16886-5
ISO10993-10等同于国标的GB/T16886-10
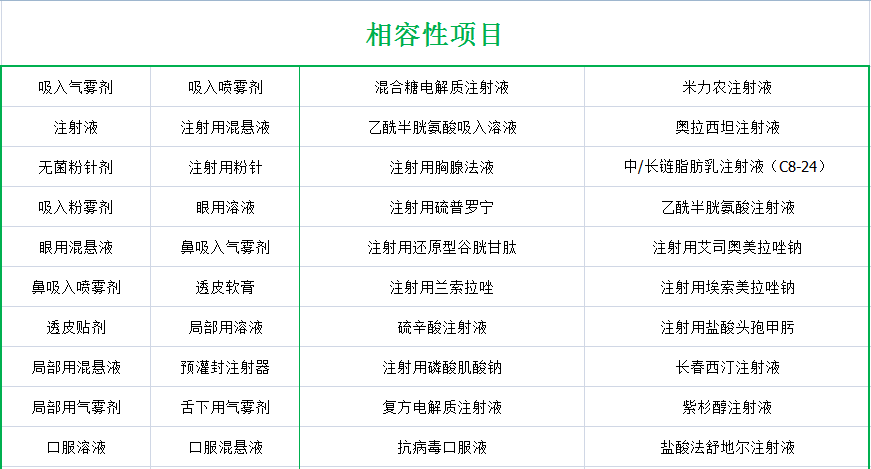
药包材相容性检测范围:

- 生物相容性检测标准 2024-05-18
- 传感器防爆合格证哪里可以办理? 2024-05-18
- 情趣用品ROHS检测报告办理? 2024-05-18
- 皮革检测报告怎么办理? 2024-05-18
- LED太阳能灯ROHS认证 2024-05-18
- 电子协调器ROHS认证 2024-05-18
- 手机消毒盒ROHS认证 2024-05-18
- 3D扫描仪ROHS认证 2024-05-18
- LED数码屏ROHS认证 2024-05-18
- 高拍仪ROHS认证 2024-05-18
- 激光测距仪ROHS认证 2024-05-18
- USB摄像头ROHS认证 2024-05-18
- 打印机ROHS认证 2024-05-18
- 触摸屏线ROHS认证 2024-05-18
- 射频控制器ROHS认证 2024-05-18
联系方式
- 电 话:13316413068
- 经理:陈小姐
- 手 机:13316413068
- 微 信:CHENYINGJUN-05







